Onde o Particelle: come immaginarsi il mondo subatomico
Dopo aver discusso della dualità onda-particella, risulta naturale chiedersi come sia possibile immaginare, visualizzare nella propria mente il mondo subatomico. È un’impresa difficile, ma non impossibile. Generalmente, gli studenti di Fisica approcciano il problema nella maniera più sensata possibile: usando la matematica. In questo modo si ottiene la comprensione più adeguata, che consente di immaginare geometricamente ciò che si sta studiando. La comprensione fisica viene con il tempo e con l’esperienza, con l’accostamento dei concetti matematici alle osservazioni fisiche che ci si aspetta di ritrovare negli esperimenti.
In puro spirito scientifico è bene armarsi di domande per imbarcarsi in questo viaggio mentale nel mondo governato dalla Meccanica Quantistica:
- su cosa è basata la nostra immaginazione, e in che modo ciò ci ostacola dal figurarci i fenomeni in modo corretto?
- quali sono i concetti utili e quali sono quelli dannosi?
- cosa definisce un oggetto?
- c’è una corrispondenza tra un fenomeno quantistico e uno classico?
Queste domande consentono a coloro che non hanno le basi per seguire un corso di Meccanica Quantistica di arrivare ad immaginare cosa succede nel mondo microscopico.
Immaginazione e comprensione
La prima cosa da notare è che la nostra immaginazione è fatta per figurarci oggetti, concetti, e comportamenti in qualche modo simili, o almeno decomponibili in cose che rispecchiano la nostra esperienza in un modo o nell’altro. A tale proposito è fondamentale ricordare che viviamo in uno spazio molto limitato di parametri fisici. In altre parole, la vita, umana e non, è possibile in un intervallo molto limitato di temperatura, pressione, velocità, accelerazione, massa e dimensioni. Ciò significa in prima battuta che, escludendo in un primo momento la scienza e i suoi successi, la nostra esperienza è fortemente limitata. Di conseguenza anche la nostra immaginazione è legata a tali limiti, ma al contempo è lo strumento per superarli, grazie innanzitutto al connubio tra pensiero matematico e pensiero fisico dal punto di vista teorico, e dalle sperimentazioni in quello pratico.
Cosa bisogna lasciarsi indietro?
Un altro ostacolo è rappresentato dalla permanenza di concetti che permeano il mondo macroscopico, ma che smettono di esserlo alle piccole scale. Il primo esempio è l’impenetrabilità dei corpi. A livello macroscopico questo è uno dei concetti più basilari, per questo motivo il volume è una proprietà fondamentale nella descrizione di un oggetto. A livello microscopico è però dovuto alla repulsione elettrostatica dovuta all’interazione di cariche dello stesso segno. Ciò comunque non deve essere necessariamente sempre vero: un elettrone ha una probabilità non nulla di trovarsi all’interno del nucleo, per esempio.
Un’altra cosa da tenere in conto è che le caratteristiche di un corpo sono fortemente contingenti. La forma, il colore, il volume e le altre caratteristiche di un qualsiasi oggetto sono determinate dai parametri fisici sopra nominati. Sebbene la frase “la lama del coltello è grigia” ci suoni perfettamente ragionevole, in realtà sarebbe corretto dire “la lama del coltello è grigia a meno di non superare gli 700°C”. Un altro esempio è costituito dai palloncini: la loro forma e dimensione sono fortemente determinati dalla pressione a cui sono sottoposti. In modo perfettamente analogo, un elettrone si comporterà in modi estremamente differenti a seconda del fatto che esso sia legato ad un atomo, che viaggi nel vuoto o addirittura in un materiale.
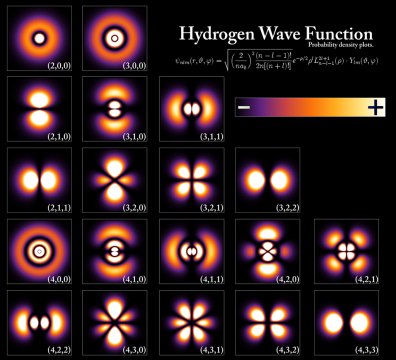
Alcuni degli stati possibili dell’elettrone legato ad un protone. [Wikipedia]
Non solo, le proprietà stesse dell’elettrone sono determinate dalla sua energia, quindi dal connubio velocità – posizione. Le caratteristiche di un ente che segue le leggi della Meccanica Quantistica sono tutte sintetizzate dallo stato: in pratica, la descrizione più approfondita di una particella: come e quanto veloce si muove, dove è più probabile trovarla, se ha o no un centro di rotazione. Lo stato trova la sua descrizione matematica nell’equazione di Schrödinger.
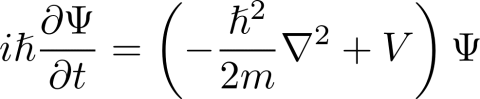
La famosa e ampiamente celebrata equazione di Schrödinger.
Si può dire perciò che lo stato è la descrizione più completa possibile di una particella data la nostra conoscenza del sistema. In pratica, sapendo a quali forze è sottoposto l’ente in questione, lo stato fornisce la descrizione migliore del suo comportamento quantistico. Il potere di previsione, naturalmente, è strettamente legato alle informazioni possedute nella costruzione dell’equazione. Ci sono sistemi più complessi che non possono essere semplicemente descritti dall’equazione di Schrödinger, descritti per esempio da quella di Dirac.
Indeterminazione
Assieme alla dualità onda-particella, il principio d’indeterminazione è la grande star della Meccanica Quantistica, e anche il suo concetto più controintuitivo. L’impossibilità di misurare simultaneamente posizione e velocità di una particella si può comprendere molto bene con un esperimento mentale: si immagini di dover vedere un elettrone. L’unico modo per vederlo è fare in modo che esso venga colpito da della luce, e che essa, rimbalzando, arrivi al nostro occhio, o strumento di misura che dir si voglia. La luce però trasporta energia, e rimbalzando sull’elettrone ne cederà una parte a quest’ultimo, perturbando lo stato iniziale. Tanto meglio lo si vuole visualizzare, tanto dev’essere energetica la luce e più grande sarà la perturbazione dell’elettrone. Si ha in questo modo indeterminazione sulla velocità. Se si vuole al contrario avere informazioni sulla velocità sarà necessario usare della luce poco energetica, ma ciò porterà per contro ad avere indeterminazione sulla posizione.
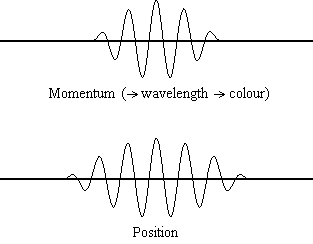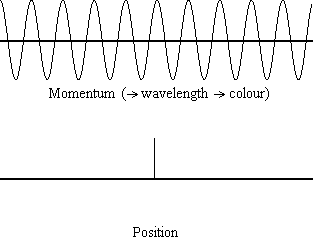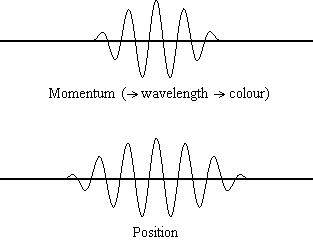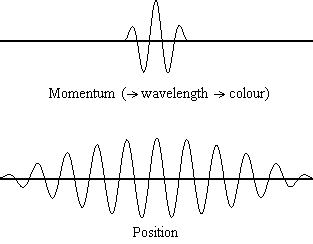
Principio di indeterminazione. Per momentum s’intende la quantità di moto, che fornisce informazioni sulla velocità. [Multiplication by Infinity]
Tutto ciò è più facile da comprendere nell’ottica della particella come onda, poiché dovrà essere localizzata in una regione spaziale invece che in un solo punto, cosa che rende indubbiamente difficile visualizzare una particella come un elettrone a meno che non si voglia immaginare la particella come un corpo esteso. Invece dell’interpretazione classica (in quest’articolo omessa) che presenta l’onda come un’onda di probabilità (più è alta la cresta più è probabile trovare la particella in quel punto), si può pensare all’onda come la particella stessa (questo tipo di interpretazione si basa sull’interpretazione Bohmiana della meccanica quantistica e, sebbene condivisa dall’autore dell’articolo, non è dimostrabile in modo certo e potrebbe cambiare nel tempo) e ciò equivale a pensare la particella come ad un corpo esteso invece che puntiforme. Quest’interpretazione facilita notevolmente le cose, anche se presenta alcuni problemi:
- L’estensione di una particella è virtualmente infinita. Sebbene maggior parte della particella sia ben localizzata, ci sarà sempre una porzione infinitamente piccola della stessa a grandi distanze.
- La forma e dimensione di una particella stessa dipendono fortemente dalla sua energia. Basti tornare alla figura delle funzioni d’onda dell’idrogeno. Le immagini, secondo quest’interpretazione, sarebbero le forme diverse che può assumere un elettrone al variare della sua energia. Ciò è comunque in accordo con quanto discusso prima sulla contingenza delle caratteristiche fisiche di un oggetto.
In sintesi, invece di pensare alle particelle subatomiche come a una pallina dura, le si possono immaginare sparpagliate in una nuvola multiforme. Naturalmente questo è solo uno dei tanti modi per figurarsele, ma elencare tutte le altre interpretazioni o estensioni presenta il serio rischio di perdersi. Per concludere, tenendo a mente queste informazioni, il mondo subatomico continuerà ad essere esotico a noi esseri macroscopici ma di certo sarà molto meno un’utile astrazione per ottenere risultati reali, pur rimanendo un mondo molto vasto. Citando Feynman:“There’s plenty of room at the bottom.” Ovvero “La in fondo è pieno di spazio”, e per questo continueranno ad arrivare articoli a riguardo. Stay tuned.
Related posts:
About Denny Trimcev
Eterno studente di Fisica. Momentaneamente devoto al culto dei formaggi, delle baguettes e del vino.
Related posts
-
La scienza non è divertente: perché i ...
3 Aprile 2017
-
A riveder le stelle: perché ci piace ...
28 Febbraio 2017
-
Oceania: l’ultima folle fatica nel mondo dell’animazione
25 Dicembre 2016
-
Democrazia e Social Network: chi la spunterà?
3 Dicembre 2016
-
Onde o particelle?
3 Novembre 2016
About Denny Trimcev
Eterno studente di Fisica. Momentaneamente devoto al culto dei formaggi, delle baguettes e del vino.